Interventi
Ginocchio
Dott. Francesco Di Caprio
Specialista in ortopedia e traumatologia
Specialista in ortopedia e traumatologia
Trattamento delle lesioni osteocondrali
Questa tecnica è stata ideata da Steadman nel 1992 e utilizza punte coniche con varie angolazioni che permettono di raggiungere artroscopicamente la sede della lesione. La procedura prevede una pulizia della cartilagine residua fino alla esposizione dell’osso sub-condrale sano; quindi con le punte vengono praticati 3 o 4 fori per centimetro quadrato, raggiungendo una profondità di 3-4 mm.
Tale tecnica permette di richiamare alla superficie articolare le cellule multipotenti contenute nell’osso spongioso. Queste ultime, venute a trovarsi in ambiente articolare, si differenziano in condrociti e producono matrice cartilaginea.
Le artroscopie di controllo eseguite nei pazienti trattati con tali metodiche hanno confermato che il difetto osteo-condrale era stato colmato da tessuto fibro-cartilagineo ben modellato e che dunque la continuità della superficie articolare era effettivamente ristabilita. Nonostante la fibro-cartilagine riparativa non sia equiparabile alla cartilagine jalina nativa in termini di qualità meccaniche, essa è in grado di sopportare i carichi e di distribuirli convenientemente a livello dell’intera superficie articolare.
Con questa metodica è possibile raggiungere ottimi risultati a distanza di un anno dall’intervento chirurgico, a fronte di un progressivo deterioramento dei risultati clinici con il trascorrere del tempo.
Allo stato attuale delle conoscenze si può affermare che l’indicazione specifica per le tecniche di stimolazione midollare è rappresentata dalle lesioni croniche di piccola estensione.
Grazie allo sviluppo dell’ingegneria tissutale è stato recentemente possibile sviluppare tecniche di medicina rigenerativa anche per le lesioni osteo-condrali: il principio è quello di sfruttare le capacità delle cellule di differenziarsi e di replicare, al fine di ricostituire tessuti del tutto analoghi a quelli lesionati.
Trapianto di condrociti autologhi
La tecnica del trapianto di condrociti autologhi è stata sviluppata in origine a partire dagli esperimenti sulle lesioni focali osteo-condrali dei conigli da Grande et al. nel 1989. Essi dimostrarono che, nei difetti in cui era stato effettuato il trapianto, era stata ricostruita una significativa porzione di cartilagine (82%) contrariamente a quanto accaduto nel gruppo di controllo in cui non era stato eseguito il trapianto (18%). La svolta nell’applicazione del trapianto di condrociti autologhi nel ginocchio umano fu rappresentata dai dati riportati da Brittberg et al. nel 1994. Grazie allo sviluppo di innovativi scaffold biodegradabili, è stato possibile ottenere al termine della fase di laboratorio un costrutto in forma di membrana, impiantabile per via artroscopica, contenente al suo interno i condrociti autologhi coltivati.
Trapianto di cellule staminali midollari
Il trattamento artroscopico delle lesioni osteo-condrali mediante trapianto di condrociti autologhi ha dimostrato di ottenere buoni risultati clinici e istologici, a fonte di una limitata invasività chirurgica. Tuttavia i limiti di questa tecnica sono la necessità di due interventi chirurgici e di un laboratorio attrezzato per la coltura cellulare con relativi costi.
Allo scopo di identificare una popolazione cellulare da utilizzare per la rigenerazione di lesioni condrali o osteo-condrali, anche al fine di ovviare alle tecniche di espansione cellulare, l’attenzione è stata recentemente rivolta alle cellule staminali che possono rigenerare vari tipi di tessuto. Le cellule staminali rappresentano una popolazione presente nella maggior parte dei tessuti adulti. Esse partecipano all’omeostasi del tessuto e sono fondamentali per la vitalità, il mantenimento e la risposta agli insulti esterni. Esse sono la fonte di tutti i tessuti neoformati nei processi riparativi e di rimodellamento, e sono guidate nelle loro attività da molecole-segnale che controllano la loro attivazione, proliferazione, migrazione, differenziazione e sopravvivenza. Una caratteristica molto interessante è la multipotenzialità delle cellule staminali, cioè la capacità di differenziarsi virtualmente in qualunque altro tipo di tessuto: le cellule staminali derivate da osso, midollo osseo, muscolo e grasso, hanno dimostrato di potersi differenziare in multipli fenotipi, incluso quello osseo, cartilagineo, tendineo, ligamentoso, adiposo, muscolare e nervoso. Le fonti di cellule staminali per il tessuto muscolo-scheletrico sono molte, e includono il midollo osseo, il periostio, la cartilagine, il muscolo, il grasso e i periciti vascolari. La possibilità di prelievo da questi tessuti è influenzata dalle complicazioni che inevitabilmente la manovra comporta. In particolare l’aspirazione di midollo osseo è associata alla minore morbilità, e permette di ottenere una sospensione cellulare che può essere rapidamente processata, anche intra-operatoriamente per un immediato reimpianto.
Per quanto riguarda i biomateriali disponibili come scaffold per l’impianto e la crescita cellulare ve ne sono innumerevoli, i quali devono rispondere a determinate caratteristiche: porosità, biocompatibilità, biodegradabilità, adesività per le cellule da veicolare. Tra questi la membrana di acido ialuronico, già utilizzata per il trapianto di condrociti autologhi, ha suscitato notevole interesse. Essendo costituito da acido ialuronico, i prodotti di degradazione di questo biomateriale non risultano citotossici, ma sono in grado di svolgere effetti positivi per la crescita e l’attecchimento della componente cellulare trapiantata.
Per quanto riguarda le molecole segnale, quelle principalmente implicate nella differenziazione in senso cartilagineo delle CSM sono TGF-beta e IGF-1. Entrambi sono facilmente reperibili nel gel piastrinico, prodotto con metodo automatizzato a patire da sangue venoso autologo. Numerosi autori hanno dimostrato l’utilità del gel piastrinico nel favorire la replicazione cellulare, la rigenerazione ossea e di numerosi altri tessuti.
Ricostruzione legamento crociato anteriore (LCA)
Il legamento crociato anteriore (LCA) è uno dei legamenti del pivot centrale del ginocchio. Esso origina dall’aspetto mediale del condilo femorale laterale, e si inserisce sulla parte antero-mediale della spina tibiale. La funzione primaria del LCA è di contrastare la traslazione anteriore della tibia rispetto al femore. Inoltre interviene come stabilizzatore secondario nei confronti delle rotazioni e dei movimenti in varismo e valgismo. La traslazione anteriore della tibia viene provocata principalmente dalla contrazione del muscolo quadricipite. Il LCA viene coadiuvato nella sua funzione da altri stabilizzatori, divisi in statici (menisco mediale, legamenti collaterali) e dinamici (flessori del ginocchio, bendelletta ileo-tibiale). Gli stabilizzatori secondari sono più efficaci con il ginocchio flesso, mentre intorno ai 20° di flessione essi si trovano in posizione inefficace: il LCA viene infatti lesionato in seguito a traumi distorsivi che solitamente avvengono in rotazione, con il ginocchio flesso di circa 20°.
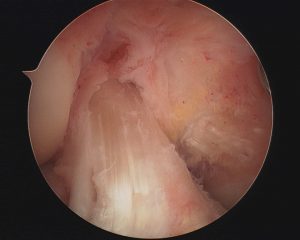
Il LCA è un legamento intra-articolare: da ciò ne consegue un particolare comportamento biologico per cui, una volta lesionato, il legamento non è in grado di cicatrizzare. Sono possibili 3 gradi di lesione:
- I grado: distrazione del legamento senza interruzione delle fibre
- II grado: lesione parziale
- III grado: lesione completa
Le lesioni di grado I non meritano un trattamento chirurgico. Le lesioni di grado II vanno operate solo in pazienti giovani con elevate esigenze funzionali, in quanto in questi ultimi la lesione tende a diventare completa. Le lesioni di grado III sono solitamente chirurgiche, a meno che non si tratti di ginocchia artrosiche, nel qual caso il trattamento dell’artrosi ha la precedenza sul trattamento della lesione legamentosa.
La storia naturale di un ginocchio con lesione del LCA porta a un instabilità cronica, con episodi distorsivi più o meno frequenti, lesioni meniscali e danno cartilagineo progressivo. Per evitare queste sequele è necessario il trattamento chirurgico della lesione.
La lesione del LCA in fase acuta richiede un trattamento iniziale con un tutore articolato, per evitare movimenti torsionali del ginocchio, risolvere l’emartro e permettere la cicatrizzazione degli stabilizzatori secondari eventualmente danneggiati. In questa fase il carico può essere concesso, se non in presenza di danni cartilaginei. Dopo 3 settimane si possono iniziare gli esercizi di recupero funzionale e muscolare del ginocchio.
Si ritiene che una buona riabilitazione pre-operatoria faciliti il recupero post-operatorio.
L’intervento di sostituzione del LCA prevede l’utilizzo di un tessuto di resistenza idonea che ricostituisca il percorso intra-articolare del LCA. Questi tessuti vengono passati all’interno del ginocchio attraverso dei tunnel, e poi fissati con viti o con cambre metalliche. Questi mezzi di sintesi forniscono la stabilità primaria del neo-legamento, che è fondamentale per l’inizio della riabilitazione. Durante il periodo post-operatorio i tessuti impiantati vanno incontro a un fissaggio biologico all’osso ospite, che fornisce la stabilità secondaria, la quale viene raggiunta dopo non meno di 12 settimane. Inoltre i tessuti impiantati vanno incontro a un processo di riassorbimento e riorganizzazione cellulare, detto “ligamentizzazione”, per cui il neo-legamento si indebolisce durante il secondo-terzo mese post-operatorio, per poi riacquistare la sua resistenza meccanica: durante questo periodo è dunque fondamentale proteggere il legamento ricostruito da stress eccessivi.
I tendini utilizzati, nella maggior parte dei casi, sono prelevati dal paziente stesso (tendini autologhi), sacrificando quindi dei tendini che possono essere rappresentati dalla porzione centrale del rotuleo, oppure dai tendini gracile e semitendinoso. Il tendine rotuleo ha il vantaggio di fornire una sicura resistenza meccanica, sia per le proprietà del tendine sia per il fissaggio con viti a interferenza sulle bratte ossee, che fornisce un’ottima stabilità primaria; ha però lo svantaggio di provocare un danno all’apparato estensore, con frequente incidenza di gonalgia anteriore nel post-operatorio. I tendini gracile e semitendinoso forniscono una stabilità primaria inferiore in quanto più difficili da fissare, per cui non permettono una riabilitazione aggressiva; però creano un minor danno da prelievo. Uno svantaggio del prelievo di semitendinoso e gracile è rappresentato dall’elevata incidenza di vasti ematomi della parte posteriore della coscia e del polpaccio nel post-operatorio.
Alternative possibili sono i tendini di donatore (omologhi), che però hanno processi di ligamentizzazione, e quindi periodi di riabilitazione, più lunghi. I legamenti artificiali al momento sono scarsamente utilizzati nelle ricostruzioni primarie, in quanto causa di frequenti reazioni infiammatorie articolari.
La riabilitazione dopo ricostruzione del LCA dovrà tenere conto di tutti questi fattori.
Periodo post-operatorio precoce
Nell’immediato post-operatorio il paziente riposa a letto con un bendaggio elastico e un tubo di drenaggio articolare, che vengono rimossi il giorno successivo all’intervento. In seguito viene posizionato un tutore rigido. Il tutore va indossato per 2 settimane durante il sonno e la deambulazione, ed ha la funzione di mantenere l’estensione del ginocchio, evitando che il paziente assuma atteggiamenti in flessione.
Il giorno dopo l’intervento il paziente può inoltre assumere la posizione seduta e alzarsi con stampelle e tutore, caricando parzialmente sull’arto operato per andare in bagno.
Dopo l’intervento il paziente rimane ricoverato per 1-2 giorni, durante i quali occorre:
- Recuperare le funzioni autonome (minzione, canalizzazione intestinale)
- Controllare eventuali stati febbrili
- Controllare il dolore
- Ridurre la tumefazione articolare mantenendo la posizione in scarico e il ghiaccio locale
Durante il primo mese gli obiettivi principali sono la risoluzione dell’emartro il recupero del movimento. È importante che il paziente sia cosciente che la mobilizzazione precoce è fondamentale per evitare la formazione di aderenze che renderebbero più difficile il recupero.
Gli esercizi di mobilizzazione devono essere progressivi in base al dolore e alla tumefazione articolare, e devono curare sia il recupero della flessione che il mantenimento della completa estensione. Occorre considerare che la perdita della completa estensione è più difficile da recuperare rispetto alla flessione, e che questo difetto compromette la stazione eretta e la deambulazione corretta.
In questo periodo gli esercizi possono anche essere eseguiti in maniera autonoma, poiché non è cruciale l’aiuto di un fisioterapista.
- Mobilizzazione passiva con apposito mobilizzatore aumentando progressivamente l’arco di movimento
- Contrazioni isometriche del quadricipite per il mantenimento dell’estensione completa
- Al termine dei 15 gg. viene effettuata la desutura della ferita
Il tutore viene abbandonato dopo 2 settimane.
Anche in questo periodo l’obiettivo principale è il recupero del movimento. Dopo la desutura è però possibile introdurre nuovi esercizi:
- Ginnastica in acqua
- Chinesiterapia con l’aiuto di un terapista (occorre prestare molta attenzione al recupero completo dell’estensione, che è fondamentale per la normale deambulazione)
- Mobilizzazione trasversa della rotula
- Elettrostimolazioni
- Stretching degli ischio-crurali e del polpaccio
Le stampelle possono essere abbandonate dopo 3 settimane, e il carico libero può essere ripreso.
Durante questo periodo vengono gradualmente introdotti esercizi più complessi per il recupero della forza e della propriocettività:
- Cyclette
- Camminata su tapis roulant
- Esercizi di rinforzo con elastici di quadricipite, ischio-crurali, adduttori e abduttori
- Ginnastica propriocettiva
Durante questo periodo vengono intensificati gli esercizi di rinforzo muscolare, introducendo esercizi a catena cinetica chiusa. Questo in considerazione del fatto che prima dei 3 mesi il legamento subisce una fase di indebolimento legata al processo di ligamentizzazione.
Durante questo periodo vengono gradualmente introdotti esercizi più complessi per il recupero della forza e della propriocettività:
- Corsa su tapis roulant e successivamente su terreno piano
- Esercizi di rinforzo a catena cinetica aperta
Durante questo periodo vengono introdotti esercizi specifici per lo sport praticato:
- Esercizi con il pallone
- Corsa sul campo, con graduale introduzione di salite, corsa in cerchio, tragitti a 8, cambi di direzione
Durante il sesto mese si riprende gradualmente l’allenamento con la squadra, con l’obiettivo di riprendere l’agonismo dopo 6 mesi.
Le tappe descritte rappresentano la media dei pazienti, ma è importante essere consapevoli che bisogna adattare il percorso riabilitativo alle esigenze del singolo paziente, alla presenza di dolore e di versamento, aggiungendo all’occorrenza terapie aggiuntive quali, ad esempio, la laserterapia.
È altrettanto fondamentale rispettare i tempi biologici del legamento ricostruito, come descritto in precedenza, e infine la meccanica dei muscoli che agiscono sul ginocchio: i flessori hanno infatti un’azione adiuvante sul LCA, mentre la contrazione del quadricipite tende a traslare anteriormente la tibia, e pertanto va recuperata con più cautela.
Tendinopatie del rotuleo
Il tendine rotuleo è una struttura fibrosa che trasmette la forza generata dal quadricipite, dalla rotula alla tuberosità tibiale sulla quale si inserisce. È un tendine grosso e robusto, in quanto soggetto a sollecitazioni molto forti durante la corsa.
Il termine tendinopatia include tutta una serie di condizioni patologiche a carico del tendine e delle strutture che lo circondano, che vanno dalle semplici condizioni infiammatorie acute (tendinite o peritendinite) alla patologia cronica che porta alla degenerazione tendinea, la quale prende il nome di tendinosi. Questa comporta la perdita della normale struttura collaginea, che viene sostituita da tessuto amorfo con eventuali calcificazioni al suo interno, conducendo alla diminuzione di resistenza del tendine. Il tendine in questa fase si presenta dolente e aumentato di volume e rischia di andare incontro a rottura.
Tale condizione è di frequente riscontro tra gli sportivi, tanto da raggiungere una prevalenza del 14,2% tra tutti gli sportivi, e in particolare del 31,9% tra i giocatori di basket e del 44,6% tra i giocatori di pallavolo. L’evidente correlazione con l’attività del salto ha portato alla denominazione di “ginocchio del saltatore”. Tipicamente la lesione interessa la parte prossimale posteriore del tendine, in prossimità del polo inferiore della rotula.
L’eziopatogenesi è multifattoriale: sono riconosciuti fattori estrinseci e intrinseci. Tra i fattori estrinseci il principale è il microtraumatismo, l’attività fisica con stress ciclico sul tendine: sono infatti determinanti un’attività sportiva che comporti il salto il numero di ore settimanali di allenamento, il tipo di calzature e di terreno. Tra i fattori intrinseci sono riconosciuti il peso corporeo, la presenza di malallineamenti rotulei, la presenza di malformazioni del polo inferiore della rotula, la maggior performance nel salto, la rigidità muscolare, la ridotta dorsiflessione della caviglia (importante nella prima fase della ricaduta).
È importante tenere conto del fatto che il tendine è un tessuto scarsamente irrorato, e che pertanto presenta un metabolismo molto lento: per questo i processi di guarigione avvengono molto lentamente.
La tendinopatia del rotuleo è una patologia ad andamento subdolo, che esordisce gradualmente con dolore, dapprima solo durante gli sforzi maggiori, ma che poi progredisce divenendo costante anche durante la vita quotidiana o a riposo. A causa del suo andamento insidioso l’atleta si rivolge alle cure mediche solo quando i sintomi divengono insistenti, quindi quando il quadro anatomo-patologico è già avanzato, tale da richiedere tempi di guarigione piuttosto lunghi.
La terapia delle tendinopatie del rotuleo è generalmente non chirurgica, e può essere medica, fisica o riabilitativa. La terapia chirurgica comprende numerose tecniche, che non garantiscono un risultato ottimale e che prevedono tempi di recupero comunque lunghi; perciò questa opzione viene riservata ai casi refrattari, dopo il fallimento di un protocollo riabilitativo ben condotto per la durata di 6 mesi.
La terapia medica si avvale dei FANS (anti-infiammatori non steroidei), il cui utilizzo suscita però molti interrogativi in quanto sappiamo che la patologia ha un substrato infiammatorio solo nelle fasi iniziali, per cui questi sono in grado di influire sul decorso della patologia soltanto in fase di esordio. I corticosteroidi, utilizzati generalmente per via locale, ottengono un buon effetto anti-infiammatorio ma possono causare un ulteriore indebolimento del tendine, e vanno pertanto limitati a periodi di utilizzo molto brevi.
Negli ultimi anni si sta affermando l’utilizzo dell’ossigeno-ozono terapia: quest'ultima consiste in infiltrazioni locali di una miscela gassosa di ossigeno e ozono in grado di stimolare il rilascio di ossigeno dal sangue al tessuto tendineo, favorendone il recupero. Il vantaggio di questa procedura è che si pratica semplicemente in ambulatorio, che non prevede l’uso di farmaci e che agisce direttamente sulla causa della tendinosi, ossia il lento metabolismo del tendine.
Un’ulteriore opportunità terapeutica viene fornita dalla medicina rigenerativa. Questa prevede delle infiltrazioni con concentrati piastrinici estratti dal sangue del paziente stesso (gel piastrinico o PRP – PlateletRich Plasma): le piastrine, una volta iniettate, rilasciano dei “fattori di crescita”, ovvero delle molecole in grado di stimolare la rigenerazione dei tessuti.
La terapia fisica consiste nell’utilizzo di laser e ultrasuoni: entrambe hanno effetto anti-infiammatorio. Inoltre, somministrando calore profondo, stimolano l’apporto sanguigno al tendine e ne accelerano il recupero.
La terapia riabilitativa consiste nella riduzione dei carichi sportivi, evitando le attività che causano dolore; l’immobilità assoluta è controindicata in quanto è noto che la tensione è importante per indurre una corretta riorganizzazione delle fibre tendinee. L’esercizio di rinforzo eccentrico si è dimostrato superiore a quello concentrico in termini di risultati clinici. Importanti sono gli esercizi di stretching, ma controindicati in fase acuta. Può essere utile la massoterapia. L’uso del ghiaccio locale è indicato subito dopo l’attività fisica.
Il ritorno all’attività sportiva può avvenire nell’arco di 2-4 settimane per i casi acuti (tendinite), mentre se si instaura un processo degenerativo a carico del tendine (tendinosi), sono necessari 4-6 mesi.
Chirurgia protesica del ginocchio
Il ginocchio è un’articolazione complessa che sopporta gran parte del peso corporeo, e che deve conciliare una grande stabilità per resistere al carico, con una notevole mobilità. Esso è costituito da tre compartimenti articolari: le articolazioni femoro-tibiali mediale e laterale, e la femoro-rotulea.
Le prime sono composte dai due condili femorali che si articolano con i corrispondenti piatti tibiali, tramite l’interposizione dei due menischi; su queste articolazioni si distribuisce il peso corporeo. La femoro-rotulea permette invece lo scorrimento dell’apparato estensore (e quindi della rotula) sul femore durante la flessione del ginocchio.
Come in ogni articolazione, i capi articolari sono rivestiti da uno strato di cartilagine di 4-5 mm di spessore. La cartilagine è un rivestimento liscio e duro, che permette ai capi articolari di scorrere uno sull’altro nell’arco del movimento. La cartilagine è un tessuto che presenta capacità rigenerative approssimativamente nulle: questo significa che il danno cartilagineo è perlopiù irreversibile; quando una lesione della cartilagine si instaura, questa causa un aumento dell’attrito sulla cartilagine residua, che ne accelera il consumo, rendendo il danno progressivo, fino all’eventuale artrosi.
L’artrosi di ginocchio può avvenire per varie cause:
L’artrosi primaria è la più comune, manon ha una causa riconosciuta, ma è favorita dalla familiarità, dal sesso femminile, dal sovrappeso e dall’età avanzata.
L’artrosi secondaria invece è legata a cause specifiche, come le deviazioni assiali del ginocchio (ginocchio varo o valgo), gli esiti di fratture articolari, l’instabilità, le malattie reumatiche, le osteocondriti.
Non esiste una cura in grado di guarire l’artrosi, ma tutte le terapie disponibili sono semplicemente rivolte ad alleviare i sintomi e a ritardare la necessità di un eventuale intervento di protesi.
E’ importante riconoscere che la protesi di ginocchio è un intervento gravoso e con una riabilitazione impegnativa. Inoltre non è in grado di fornire risultati del 100%, ma un ginocchio protesizzato presenta sempre qualche fastidio. Per questo occorre soppesare bene la necessità di un’artroprotesi, effettuarla solo quando i sintomi realmente la giustificano, e solo dopo aver tentato tutte le terapie alternative.
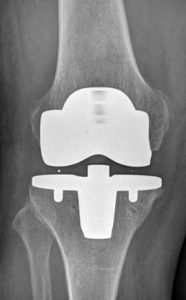
La protesi di ginocchio sostituisce le superfici articolari usurate con dei rivestimenti in materiale biocompatibile. Tra le componenti tibiale e femorale viene interposto uno spaziatore in polietilene, un materiale plastico. Qualora sia necessario protesizzare anche la rotula, anche la componente rotulea è in polietilene. Le componenti possono essere fissate all’osso con meccanismo a “press-fit”, cioè ad incastro e successiva integrazione biologica del materiale all’osso, oppure tramite cementazione delle componenti.
Esistono diversi tipi di protesi di ginocchio, che possono essere divise come segue:
Protesi monocompartimentali
Protesi parziali che sostituiscono uno solo dei tre compartimenti (più spesso il femoro-tibiale mediale). Questo tipo di protesi comporta un percorso riabilitativo più rapido, ma è attuabile solo in pazienti relativamente giovani, con danno cartilagineo localizzato ad un solo compartimento, e con legamenti normali.
Protesi bi- e tri-compartimentali
- CR: Protesi a conservazione del legamento crociato posteriore. Si tratta di protesi totali che conservano il legamento crociato posteriore per la sua funzione di perno centrale del ginocchio. Queste presentano però diversi svantaggi legati al difficile bilanciamento legamentoso, per cui sono usate raramente.
- Menisco mobile: si tratta di protesi con inserto in polietilene con libertà di movimento rotazionale rispetto alla componente tibiale. E’ una protesi che prevede il sacrificio del LCP ed un inserto ad elevata congruenza che garantisce comunque un’elevata stabilità.
- PS: Protesi a sostituzione del legamento crociato posteriore. Si tratta di protesi che sacrificano il legamento crociato posteriore, sostituendolo con un sistema di stabilizzazione posteriore del ginocchio. Questo è il tipo i protesi montato più spesso, e presuppone l’integrità dei legamenti collaterali.
- CCK: Protesi semivincolata che ha una stabilità intrinseca, indicata in caso di instabilità legamentosa o marcata deformità del ginocchio.
- Vincolata: Protesi a cerniera che permettono un solo grado di movimento. Si utilizza in caso di gravi deformità, di interventi di revisione o di malattie neurologiche che compromettono il controllo dell’arto.
In ognuno di questi casi la protesizzazione della rotula è opzionale, non fornisce benefici certi, ed è pertanto una scelta affidata all’esperienza ed alle preferenze del chirurgo.
Obiettivi generali
Gli obiettivi della riabilitazione dopo artroprotesi di ginocchio si possono riassumere come segue:
- Prevenire le complicanze post-operatorie precoci.
- Ottenere un arco di movimento pressoché completo.
- Recuperare il trofismo muscolare.
- Recuperare l’autonomia funzionale.
- Periodo post-operatorio precoce
Nell’immediato post-operatorio il paziente riposa a letto con un bendaggio elastico e un tubo di drenaggio articolare, che vengono rimossi 1-2 giorni dopo l’intervento. Il sangue eventualmente recuperato durante l’intervento viene reinfuso entro 6 ore nel post-operatorio.
Una volta rimosso il drenaggio il paziente inizia la mobilizzazione passiva del ginocchio operato, con apposito mobilizzatore. Il paziente può assumere la posizione seduta. 2-3 giorni dopo l’intervento il paziente può alzarsi con le stampelle, caricando parzialmente sull’arto operato (30% del peso corporeo).
Dopo l’intervento il paziente rimane ricoverato per 6-7 giorni, durante i quali occorre:
- Trattare l’eventuale anemizzazione attraverso ripetuti controlli dell’emocromo e terapia marziale o trasfusioni di sangue omologo o autologo.
- Recuperare le funzioni autonome (minzione, canalizzazione intestinale).
- Controllare eventuali stati febbrili.
- Controllare il dolore per mezzo di farmaci e cateteri perinervosi.
- Ridurre la tumefazione articolare mantenendo la posizione in scarico e il ghiaccio locale.
- Prevenire le complicanze circolatorie come la trombosi venosa profonda (TVP), attraverso l’utilizzo di calze elastiche e farmaci anticoagulanti.
- Una volta stabilizzate le condizioni del paziente e ristabilita una sufficiente autonomia funzionale, il paziente viene dimesso.
Durante il primo mese l’obiettivo principale è il recupero del movimento. E’ importante che il paziente sia cosciente che la mobilizzazione precoce è fondamentale per evitare la formazione di aderenze che renderebbero più difficile il recupero.
Gli esercizi di mobilizzazione devono essere progressivi in base al dolore ed alla tumefazione articolare, e devono curare sia il recupero della flessione che il mantenimento della completa estensione. Occorre considerare che la perdita della completa estensione è più difficile da recuperare rispetto alla flessione, e che questo difetto compromette la stazione eretta e la deambulazione corrette.
In questo periodo gli esercizi possono anche essere eseguiti in maniera autonoma, e non è fondamentale l’aiuto di un fisioterapista.
Mobilizzazione passiva con apposito mobilizzatore a gradi crescenti.
Contrazioni isometriche del quadricipite per il mantenimento dell’estensione completa.
Mobilizzazione attiva ai massimi gradi della caviglia dal lato operato, allo scopo di migliorare la circolazione ematica dell’arto.
Training deambulatorio con stampelle e carico parziale sull’arto operato, in piano e sulle scale.
Al termine dei 15 gg. viene effettuata la desutura della ferita.
Anche in questo periodo l’obiettivo principale è il recupero del movimento. Dopo la desutura è però possibile introdurre nuovi esercizi:
Ginnastica in acqua.
Chinesiterapia con l’aiuto di un terapista.
Mobilizzazione trasversa della rotula.
Elettrostimolazioni.
Nel periodo post-operatorio precoce va evitato il massaggio della cicatrice.
Al termine dei 30 gg. viene eseguito un controllo radiografico. Se questo sarà regolare si potrà abbandonare gradualmente le stampelle (iniziando da quella dal lato operato), compatibilmente con il dolore e con il livello di autonomia raggiunto.
Durante questo periodo vengono gradualmente introdotti esercizi più complessi per il recupero della forza, della propriocettività e dell’autonomia funzionale:
- Cyclette
- Stretching
- Esercizi di rinforzo con elastici di quadricipite, ischio-crurali, adduttori e abduttori.
- Ginnastica propriocettiva.
La riabilitazione viene gradualmente protratta fino a ottenere un recupero funzionale sufficiente, il che richiede circa 3 mesi. Il ginocchio operato di protesi, tuttavia, recupera la sua funzione lentamente, per cui il tempo necessario per un recupero completo è mediamente di sei mesi.
E’ importante tenere conto che i tempi descritti riflettono la media dei pazienti, ma che in ogni caso le terapia andranno regolate sulla base delle condizioni soggettive, del dolore, della presenza di tumefazione articolare e delle eventuali problematiche generali associate.
